亮点
通过动态构象分析,以基于物理规律的方式预测大环肽的渗透性。我们引入了一种计算高效的分子动力学框架,通过量化依赖环境的构象适应性及极性表面积的特定变化,准确预测大环肽的渗透性。
“变色龙”环肽渗透性的机制洞察与预测建模
环肽的临床潜力常常受到其较差膜渗透性的限制。由于这些分子具有复杂的构象柔性,这一特性极难预测。为了应对这一挑战,我们开发了一个综合框架,将分子动力学 (MD) 模拟与机器学习相结合,以揭示被动膜转运的机制决定因素。
我们的方法通过显式建模多肽在不同溶剂环境中的动态行为,克服了传统静态描述符的局限性。我们在水相和氯仿溶剂中使用 MD 模拟来模拟膜转位过程中遇到的极性梯度。通过采用高温模拟 (490 K),我们增加了对稀有构象转变的采样,使我们能够捕捉大环肽的“变色龙”特性——它们在水中暴露出极性基团,而在非极性膜环境中则将其屏蔽。
尺寸依赖阈值与预测建模
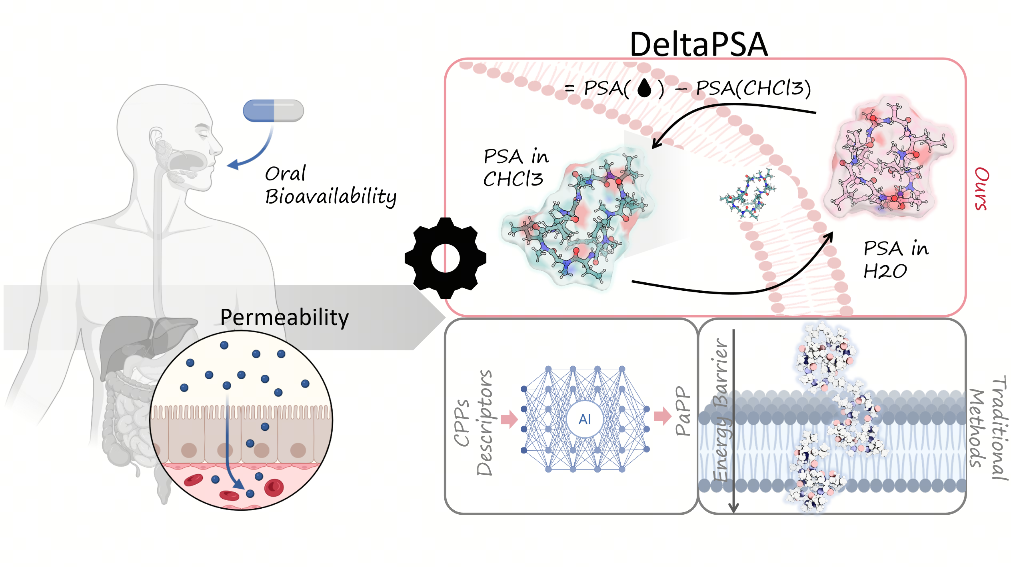
本研究的一个关键发现是确定了构象适应性的尺寸依赖阈值。我们的分析表明,单体长度为九个或更多残基的大环肽会表现出显著的溶剂依赖性构象转换。对于这些较大的大环肽,水相和类膜状态之间极性表面积的差异 (ΔPSA) 是评估其渗透性的关键定量指标。那些能够通过构象转换最小化 ΔPSA 的多肽,表现出较低的膜插入能量成本和更高的渗透率。
基于这些洞察,我们训练了机器学习模型来预测渗透性结果。随机森林分类器的 F1 分数达到了 0.86,展现出极高的预测准确性。特征重要性分析识别出两个特定的溶剂可及表面积 (SASA) 指标——水相中的非极性 SASA 和氯仿中的极性 SASA——作为膜渗透性最有力的预测因子。这些描述符直接量化了多肽通过动态结构调整来平衡溶解性和亲脂性的能力。
此外,我们还优化了计算工作流以支持高通量应用。我们证明,两次独立的 300 纳秒模拟足以提取稳健的动态特征,这与传统的增强采样方法相比大幅降低了计算成本。该框架为新生实验室提供了一个可扩展且机制明确的工具,助力细胞渗透性大环治疗药物的合理设计。